【券商薦股精選】機會已來,這類廠商有望扶搖直上,歷史估值底部,有望實現戴維斯雙擊
【碳中和動態分析】生態環境部:把光伏產業打造成標桿性行業;中車風電業務高速發展,株洲所2020年交付風電整機增長731%
近期,阿斯利康的新冠疫苗AZD1222迷霧重重,先是陷入歐洲“血栓門”,后又被美國質疑遞交過時的臨床試驗數據。
據了解,該疫苗屬于腺病毒載體技術,已在全球70多個國家獲得有條件上市授權或緊急使用。阿斯利康公布的三期臨床數據顯示,AZD1222在預防癥狀性新冠肺炎方面有效率為79%,預防嚴重疾病和住院治療的有效率為100%。
對于AZD1222近期的風波,阿斯利康中國區相關負責人對《華夏時報》記者表示,所有可披露的信息以阿斯利康官網為準。

該疫苗的中國代理權由康泰生物取得。2020年8月,阿斯利康與康泰生物簽署了中國內地市場獨家授權合作框架協議,康泰生物負責其在中國內地市場的研發、生產、供應和商業化。
康泰生物正在積極推動該疫苗在國內的臨床注冊事宜。此前,申萬宏源研報認為,康泰生物將在國內開展橋接試驗,根據橋接試驗的時間推算,該疫苗有望于2021年下半年在國內上市。不過,尚不知道AZD1222目前的數據風波是否會延緩其在國內的上市進度。
疫苗專家陶黎納(疫苗與科學)在接受本報記者采訪時表示,即便是安全性和效果均已得到證實的mRNA疫苗,復星醫藥在引進的時候也不太順利。而腺病毒載體疫苗,康希諾的產品已經獲批上市,阿斯利康的這一款并不能填補國內的技術空白,再加上近期的負面事件,或將引發公眾接受度下降。“我不知道國家藥監局會不會考慮公眾接受度,如果考慮到這個因素,不給通過(審批)的可能性也是存在的。”
發生“血栓門”一度被近20國叫停
在本月初,AZD1222現“血栓門”。由于丹麥、挪威等地出現醫護人員接種后發生出血、血栓和血小板數量降低的癥狀,包括德國、法國、丹麥、挪威、冰島、意大利、泰國、奧地利等近20個國家一度叫停阿斯利康疫苗接種。
據科技日報報道,3月3日,在德國一家診所工作的護士接受了第一劑阿斯利康疫苗的接種。7至8天后,她出現嚴重的頭疼癥狀并住進了醫院。3月20日,這名55歲的女護士不幸病世。醫生認為導致護士死亡的腦靜脈血栓與疫苗接種相關的可能性很高,并將有關情況報告了德國負責疫苗安全的保羅·埃爾利希研究所(PEI)。如果得到證實,該護士將是德國報告的第15個此類病例。
關于阿斯利康疫苗可能導致部分接種者產生血栓的原因,德國格萊夫斯瓦爾德大學的研究人員通過對6名血栓患者的血樣研究發現,人體自身的抗體是對疫苗的強烈免疫反應的一部分,可能會錯誤地與血小板結合并觸發大量的血小板活化,從而導致罕見的竇靜脈血栓形成。但目前尚不清楚這一反應是由于疫苗本身還是載體造成的,或者可能是作為疫苗免疫反應的一般性炎癥反應。
不過,世界衛生組織及歐洲的監管部門審查后認為“血栓與阿斯利康疫苗的因果關系尚未確立”“該疫苗的益處仍大于風險”。目前該疫苗已在歐洲恢復接種。
3月18日,歐洲藥品和保健品監管局(MHRA)公布了對英國1100多萬接受阿斯利康新冠疫苗接種后,發生血栓的審查結果。其認為,沒有證據表明靜脈中的血栓發生率超過了未接種疫苗時的預期。目前在英國接種疫苗的人中,只有不到百萬分之一的人報告了這種情況,與疫苗的因果關系尚未確立。
歐洲藥品管理局(EMA)的藥物警戒風險評估委員會亦得出結論:阿斯利康的新冠疫苗沒有增加血栓的總體風險。但對于極少數伴有血小板減少的嚴重血栓栓塞事件,雖然不能證明與疫苗的因果關系,但值得進一步分析。
對此,阿斯利康表示將繼續與有關部門密切合作,確保AZD1222的適當使用。公司認可并將落實有關部門的建議,包括更新產品信息,同時繼續了解這些事件的性質和相關性,以確保在這場公共衛生危機中繼續安全地提供疫苗。
陶黎納表示,自己對阿斯利康疫苗的安全性并不擔心。雖然從臨床試驗數據中看到,新技術路徑的腺病毒載體疫苗、mRNA疫苗,常見的不良反應率確實高于傳統技術路徑的滅活疫苗,但這些常見的不良反應都在可以接受的范圍內。不能說因為它們的發生幾率高一點,就說這些疫苗不安全。
“世界衛生組織已經表態了,說沒有證據表明阿斯利康的疫苗增加了血栓的概率。當然歐洲也有一些專家說,他們找到了阿斯利康疫苗導致血栓的證據。但我認為那些不是證據,只是一種原理的推測,雖然在醫學上可以解釋,但缺乏證據。對我個人來說,我對這款疫苗的安全性有把握。”陶黎納說。
臨床試驗數據被質疑“過時”
一波未平,一波又起。“血栓門”的余波尚未過去,美國即開始質疑阿斯利康遞交的新冠疫苗數據。
3月23日,美國國家過敏與傳染病研究所(NIAID)表示,這款疫苗有效率的報告數據可能不完整,質疑阿斯利康提交過時的臨床試驗數據。
NIAID的聲明指出,接獲美國數據安全和監測委員會(DSMB)提醒,阿斯利康提交的數據可能未反映整體狀況,其中或使用一些過期的研究數據,影響報告顯示的疫苗有效率。NIAID敦促阿斯利康與DSMB合作,審查療效數據,確保盡快公布最準確、最新的療效數據。

而關于AZD1222是否能在美國獲批緊急使用授權,將在有關部門對數據進行徹底審查后決定。對此,阿斯利康當日發表聲明稱,前一天發布的有效性數據是基于截至2月17日的中期分析,將在48小時內發布完整分析結果。
據媒體報道,DSMB曾致信阿斯利康,認為應該把有效率報為69%至75%,而不是未納入最新數據的79%。
中國合作伙伴康泰生物還好嗎?
阿斯利康新冠疫苗頻現風波,拿下其中國代理權的康泰生物還好嗎?
2020年8月,康泰生物發布公告,稱阿斯利康獨家授權公司在中國內地對AZD1222進行研發、生產及商業化。
根據合作框架協議條款約定,康泰生物作為技術受讓方將確保在2020年底前達到至少1億劑AZD1222的年產能,并在2021年底前將該疫苗設計產能擴大至年產至少2億劑,以滿足中國市場的需求。2021年2月,康泰生物腺病毒載體疫苗車間宣布落成,年產量可達4億劑。
陶黎納認為,康泰生物引進阿斯利康的這款疫苗,不是一個太好的主意。“因為它與康希諾的技術路徑相同,均屬于腺病毒載體疫苗,與復星醫藥引進mRNA疫苗不同,對它的引進不算填補國內空白。尤其是現在阿斯利康又遇到了這些問題,雖然科學上不認為這款疫苗與血栓存在因果關系,但還是會造成民眾的恐慌。”
康泰生物曾對媒體表示,公司與阿斯利康的合作方式為技術引進,產品將以中國的疫苗監管要求為標準向相關審批部門報批。公司已建立全面質量管理體系,嚴格注重產品質量問題,研發具體進展以公司公告信息披露為準。
除了阿斯利康疫苗,康泰生物亦在開發滅活疫苗。借助新冠疫苗概念,康泰生物2020年至今股價上漲超40%,股東一度減持套現。不過相比其競爭者,康泰生物新冠疫苗上市進度已然落后,競爭力有限。
目前,康希諾的腺病毒載體疫苗、國藥中生的滅活疫苗、科興中維的滅活疫苗均在國內獲批附條件上市,目前總接種量約為7500萬劑次,今年二季度接種將提速。而康泰生物的兩款新冠疫苗仍處于臨床甚至臨床前階段。

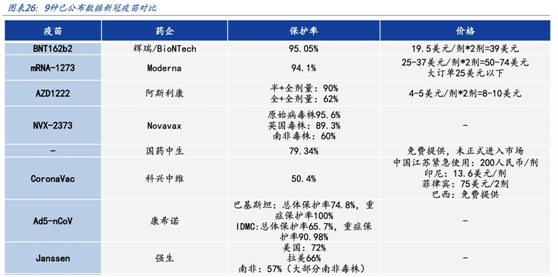 (圖片來自國盛證券研報)
(圖片來自國盛證券研報)但值得一提的是,阿斯利康這款疫苗的報價在全球是最低的,約為3-4美元/劑,需要接種兩劑,價格在60元人民幣以內,所以仍有價格優勢。“如果康泰生物在產能上占優,能夠降低成本的話,也算一個利好,就算效果稍微差一點也是可以接受的。”陶黎納說。
?

責任編輯:彭佳兵
APP專享直播
熱門推薦
收起
24小時滾動播報最新的財經資訊和視頻,更多粉絲福利掃描二維碼關注(sinafinance)














