牛市第二階段上攻蓄力中?軍工、醫藥等牛股倍出,牛市情緒仍在,你還不上車?點擊立即開戶,3分鐘極速響應,專屬福利!助你“穩抓賺錢時機”!
今日直播
原標題:A股新冠疫苗第一股來了:明天申購!發行價A股史上第二,中一簽最少賺10萬?其港股已連漲3天…
在全球新冠疫情仍舊嚴峻之際,被譽為A股新冠疫苗第一股的康希諾明天就可打新了!
目前,該股已確定A股發行價,為209.71元/股。統計數據顯示,這一發行價為科創板史上第二高,也是A股史上第二高。
與此同時,康希諾港股近日也出現異動,連續3個交易日上漲,最近兩個交易日盤中漲幅均超過10%。
A股新冠疫苗第一股來了!明天申購
根據安排,康希諾A股將于2020年7月31日,也就是明天正式進行網上申購。康希諾本次發行股票數量為 2480萬股,約占發行后公司總股本的 10.02%。
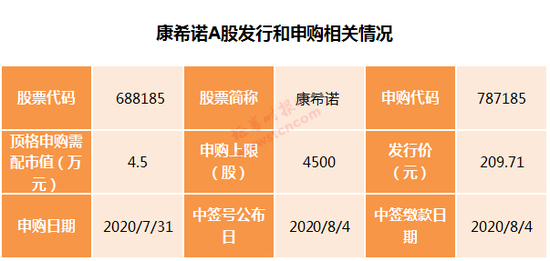
坊間將康希諾視為A股市場新冠疫苗第一股。
根據康希諾的A股發行公告,截至 2020 年 6 月 7 日,公司產品管線包括針對預防埃博拉病毒病、腦膜炎、百白破、肺炎、結核病、 新型冠狀病毒(COVID-19)、帶狀皰疹等 13 個適應癥的 16 種創新疫苗產品。其中, Ad5-EBOV 疫苗在 2017 年 10 月取得新藥證書,MCV4、MCV2 已提交 NDA 并取得受理,重組新型冠狀病毒疫苗(腺病毒載體)已完成臨床 II 期試驗,嬰幼兒用 DTcp、 DTcP 加強疫苗、PCV13i 正在進行臨床 I 期試驗,結核病加強疫苗正在進行臨床 Ib 試 驗,PBPV 正在進行臨床 Ia 期試驗,青少年及成人用 Tdcp 處于臨床批件申請階段, DTcP-Hib 聯合疫苗、CSB012-腺病毒、CSB015-腦膜炎、CSB016-帶狀皰疹、CSB017- 脊髓灰質炎、CSB013-寨卡病毒處于臨床前研究階段。
值得注意的是,康希諾此番A股發行價209.71元/股,為科創板史上第二高,也是A股史上第二高。僅次于科創板的石頭科技,其發行價為271.12元。這兩股也是截至目前僅有的發行價超過200元的股票。
而A股史上發行價超過100元的股票也僅有6只,除了海普瑞和湯臣倍健外,其他均為科創板股票。
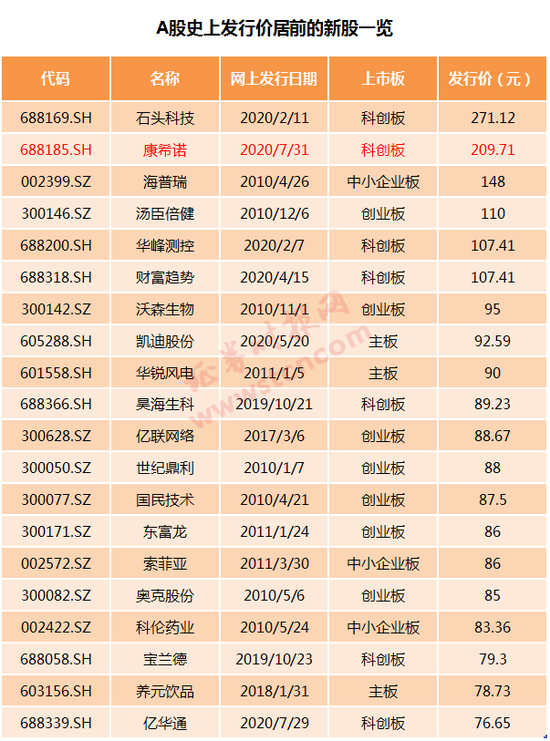
一般而言,發行價較高的新股,即便上市后漲停數較少或漲幅較小,也容易獲得較高的中簽盈利。對于科創板股票而言,也大體如此,幾只發行價居前的科創板新股中簽后盈利均較高。
由于科創板新股上市后的前5個交易日不設價格漲跌幅限制,我們通常以上市首日表現計算中簽盈利。譬如A股發行價最高的石頭科技中一簽的盈利達13.39萬元,該股首日盤中最多較發行價上漲98.76%。另一只科創板發行價較高的新股華峰測控中一簽盈利達到13.63萬元,該股首日盤中最多較發行價上漲253.78%。財富趨勢首日中簽盈利最高也接近7萬元,該股首日盤中最多較發行價上漲123.07%。上述3只發行價超過100元的科創板新股首日最高漲幅均接近或超過了100%。
總的來說,科創板新股首日表現與大市環境、個股所具有的題材概念也有一定關聯。
以康希諾A股發行價計算,如果其上市首日漲幅能達100%,則中一簽將賺超10萬元;而如果首日漲幅達200%,則一簽將賺20萬元。
不過,康希諾也給出了風險提示,公司稱,截至發行公告刊登日,埃博拉病毒病疫苗 Ad5-EBOV 已獲得新藥注冊批準,并成為中國唯一申請用作應急使用及國家儲備的埃博拉病毒病疫苗。公司其余疫苗產品處于申報上市或研發階段,公司尚未實現盈利。公司未來幾年將持續大規模的研發投入,預計上市后一段時間內將持續未盈利的狀態。本次發行存在未來股價下跌給投資者帶來損失的風險。發行人和聯席主承銷商提請投資者關注投資風險,審慎研判 發行定價的合理性,理性做出投資。
另外,康希諾本次發行也進行了戰略配售,戰略配售投資者包括中信證券投資有限公司(參與跟投的保薦機構相關子公司,以下簡稱 “中證投資”)和中金公司豐眾 18 號員工參與科創板戰略配售集合資產管理計劃(發行人的核心員工參與本次戰略配售設立的專項資產管理計劃,以下簡稱“豐眾 18 號資管計劃”)。中證投資本次獲配股票限售期為 24 個月,豐眾 18 號資管計劃本次獲配股票限售期為12 個月。
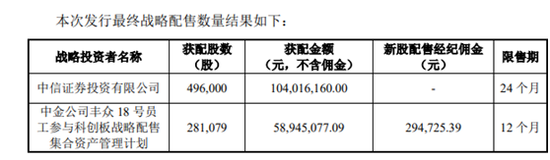
A股申購前夕 康希諾港股連續上漲
值得注意的是,在康希諾A股即將申購之際,其港股近日出現異動,連續大漲。
行情數據顯示, 7月28日至今,康希諾港股連續3個交易日上漲,漲幅分別為4.07%、11.82%和7.72%,累計上漲25.35%。
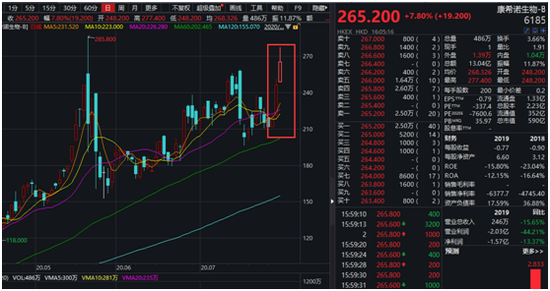
截至7月30日收盤,康希諾港股報265.00港元,按照目前匯率折算成人民幣后,較此番康希諾A股的209.71元人民幣的發行價高約14%。
由于近幾個月全球新冠疫情仍舊嚴峻,新冠疫苗的研發情況也一直牽動人心,資本市場相關公司的股價也頻頻發生異動。
比如復星醫藥近日公告稱,公司控股子公司上海復星醫藥產業發展有限公司(以下簡稱“復星醫藥產業”)收到《受理通知書》,其獲許可的新型冠狀病毒mRNA疫苗(BNT162b1)用于預防新型冠狀病毒獲國家藥品監督管理局臨床試驗注冊審評受理。復星醫藥股價近期表現堅挺,總體漲幅明顯。
此前的6月28日晚間,沃森生物公告稱,公司作為共同申報方于近日收到國家藥品監督管理局批準的新型冠狀病毒mRNA疫苗《藥物臨床試驗批件》。
而此前智飛生物也公告表示,公司收到全資子公司安徽智飛龍科馬生物制藥有限公司(以下簡稱“智飛龍科馬”或“子公司”)報告,由智飛龍科馬與中國科學院微生物研究所合作研發的重組新型冠狀病毒疫苗(CHO細胞)獲得國家藥品監督管理局臨床試驗申請受理通知書及臨床試驗批件(批件號:2020L00023、2020L00024),同意本品進行臨床試驗,該批件有效期為12個月。
在上述公告發布后不久,沃森生物和智飛生物股價都出現大幅上漲。
不過,新冠疫苗的研發并非沒有投資風險。
康希諾在招股意向書中指出,疫苗作為接種于健康人群的生物制品,安全性要求較高,生產工藝較為復雜,并需要滿足國家藥監部門的各項要求,大規模產線建設需要一定周期。即使公司重組新型冠狀病毒疫苗(腺病毒載體)研發成功,也存在公司無法在特定時間內生產出足夠數量的疫苗滿足市場需求的風險,給公司產品銷售帶來不利影響。
此外,康希諾還提示,目前尚無法準確預計世界范圍內新冠疫情的發展趨勢和各個國家抵御新冠病毒肺炎工作的最終成效。如果新冠肺炎疫情在相關疫苗開發成功之前消除,則相關疫苗將很可能不會大范圍用于人群接種,無法實現大規模商業銷售。


責任編輯:逯文云
熱門推薦
收起
24小時滾動播報最新的財經資訊和視頻,更多粉絲福利掃描二維碼關注(sinafinance)









