ذآہثط”½› > ةْ»î > ء_تدضئثژةودسë[²mةدبfثہحِ²،ہ > صخؤ
ء_تدةودسë[²m•³نNثژ²»ء¼·´‘ھ 5؟îةوتآثژ‡ّƒبسذتغ
 تذˆِ·فî~·ض²¼
تذˆِ·فî~·ض²¼
،،،،ء_تدةودسë[²m•³نNثژ²»ء¼·´‘ھ 5؟îةوتآثژخïشع‡ّƒبسذتغ Œ£¼ز·Q‡ّƒب•؛خ´°l¬F‡ہضط²»ء¼·´‘ھ
،،،،“ˆَµہ£¬س¢‡ّثژئ·؛ح½،؟µ®aئ·¹ـہي¾ض(MHRA)بصا°صشع¾o¼±ص{²éبًت؟ضئثژ¾قî^ء_تدضئثژةودسë[²m‡ہضط²»ء¼·´‘ھز»تآ£¬ثùةو¼°µؤثہحِ²،ہ¸كك_15161بث£¬ةو¼°µؤثژخïسذ8؟ئنضذ5؟îثژشعضذ‡ّسذتغ،£×ٍبص£¬ء_تد¹«ث¾½o±¾ˆَ°lپيآ•أ÷·Q£¬أ½َwˆَµہضذجل¼°µؤ²»ء¼·´‘ھتآ¼ƒHدقسعأہ‡ّز»‚€»¼صكش®ضْي—ؤ؟،£½›ك^ؤ؟ا°شu¹ہ£¬خ´°l¬FŒ¦ء_تد®aئ·µؤ°²ب«ذش®aةْس°ي‘،£
،،،،سذŒ£¼ز±يت¾£¬دàŒ¦سع‡ّح⣬ضذ‡ّبثµؤ؟‚َwسأثژ„©ء؟ئ«ذ،،£شع‡ّƒب•؛•rك€خ´°l¬Fت¹سأةدتِثژخïضآثہµب‡ہضطµؤ²»ء¼·´‘ھ£¬تآ¼‘ھش“²»•Œ¦لt¯ںسأثژشى³ة؛ـ´َ›_“ô؛ح¸ؤ׃،£
،،،،خؤ،¢±ي/س›صكذ¤ذ،في،¢ح؟¶ثسٌ
،،،،ء_تدضذ‡ّ£؛²»ء¼·´‘ھ
،،،،تآ¼ƒHدقسعأہ‡ّ
،،،،×ٍبص£¬ء_تد¹«ث¾Œ¦±¾ˆَ°lپيآ•أ÷·Q£¬أ½َwˆَµہضذجل¼°µؤ1.5بfہخ´½›°²ب«ذششu¹ہµؤ²»ء¼·´‘ھتآ¼ƒHدقسعأہ‡ّش“ي—ؤ؟،£
،،،،»ط‘ھك€½âلŒ£¬ش“تآ¼¾‰سعش“أہ‡ّ»¼صكض§³ضي—ؤ؟ضذµؤ²»ء¼تآ¼خ´¼°•rˆَ¸و£¬³ِ¬Fآ©ˆَتآ¼،£شعتآ¼°lةْ؛َ£¬ء_تدصشعإcدàêPذlةْ±O¹ـ™Cک‹أـاذ؛د×÷£¬·eکO²ةب،¸ؤص؛حîA·ہ´ëت©زش½â›Q†–î}،£ء_تد¹«ث¾»ùسعؤ؟ا°µؤشu¹ہ£¬خ´°l¬FŒ¦ء_تد®aئ·µؤ°²ب«ذش®aةْس°ي‘،£ح¬•r6شآ12بص£¬ڑWأثثژ±O¾ضشعئن¹ظ·½¾Wص¾µؤح¨¸وضذ±يت¾£¬¬FëA¶خخ´سذبخ؛خ×C“±يأ÷£¬²،بث؛حلtةْذèزھ²ةب،بخ؛خ´ëت©£»أ½َwˆَµہµؤأہ‡ّ1.5بfہثہحِ°¸ہ£¬ؤ؟ا°²»ؤـ×Cأ÷إcثژخïض±½سدàêP،£
،،،،ش“¹«ث¾ك€Œ¦±¾ˆَس›صك±يت¾£¬ةد؛£ء_تدضئثژ¹«ث¾سِµ½²»ء¼·´‘ھتآ¼•r£¬¹«ث¾Œ¢°´صصضذ‡ّµؤدàêP·¨آةزژ¶¨كMذذتص¼¯²¢ˆَ¸و½oص¸®™Cک‹،£
،،،،کIƒب£؛
،،،،îAس‹²»•Œ¦لt¯ںسأثژشى³ة›_“ô
،،،،ء_تدضئثژتاب«اٍضئثژ¾قî^ض®ز»£¬ئنثژخïµؤ²»ء¼·´‘ھتآ¼زر½›²»تاµعز»´خزٹضTˆَ¶ث،£
،،،،×ٍبص£¬ڈVضفتذµع°ثبثأٌلtش؛ش؛éLزüںëکثŒ¦±¾ˆَس›صك±يت¾£¬،°ح£ثژض®؛َ¸ْغ™°l¬F£¬°ث³ةزشةد»¼صك•³ِ¬F؟ة³ضہmذشقDêژ£¬ك@زâخ¶ضَّwƒب±û¸خ²،¶¾±»اه³£¬ك_µ½إR´²ضخسْکثœت،£،±µ«ثûز²ض¸³ِ£¬²»ء¼·´‘ھك€تاëSجژ؟ةزٹµؤ،£،°ز»ك^ذشقD°±أ¸ة¸ك،¢°×¼ڑ°û؛حرھذ،°ه½µµح،¢µôî^°l،¢´ٍلک؛َ³ِ¬F°lں،¢¹اî^ح´µب¸±×÷سأ£¬¶¼تا±بف^³£زٹµؤ£¬سذذ©زھح£ثژ£¬سذذ©„t²»±ط،£ضآثہµب‡ہضطµؤ²»ء¼·´‘ھ•؛•rك€خ´°l¬F،£،±ثû±يت¾£¬ت¹سأثژخïا°لtةْ•أ÷´_¸وضھ»¼صكسأثژ؟ةؤـ³ِ¬Fµؤ²»ء¼·´‘ھ£¬½›ح¬زâض®؛َ²إ•ت¹سأ،£
،،،،،°ك@ز»´خµؤدûد¢‘ھش“²»•Œ¦لt¯ںسأثژشى³ة؛ـ´َ›_“ô؛ح¸ؤ׃£¬زٍéك@ذ©ثژخïت¹سأزر¾أ£¬لtةْ±بف^اه³ت¹سأµؤŒچëHاé›r،£،±ضذة½´َŒW¸½Œظؤ[ءِلtش؛ثژ„©؟ئض÷بخüS¼t±ّ½é½Bصf£¬ضآثہµؤ²»ء¼·´‘ھ›]سذآ صfك^£¬صfأ÷•ّزشحâµؤ²»ء¼·´‘ھز²ف^éةظزٹ،£
،،،،تذˆِ£؛إةء_ذہ
،،،،تا½^Œ¦،°´َہذ،±
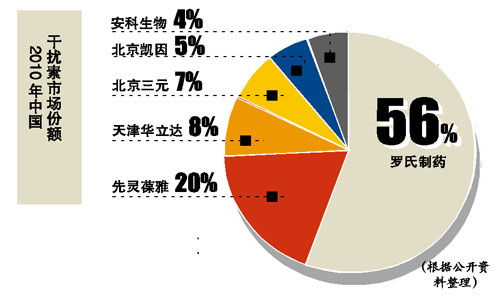
،،،،س›صكڈؤء_تدضذ‡ّ«@د¤£¬´ث´خةو¼°µؤثژخï؛صظگح،،¢أہء_بA،¢إةء_ذہ،¢°²¾Sح،،¢جطء_„Pµبخه؟îثژشعضذ‡ّ¶¼سذتغ،£¶ّ“ءث½â£¬أہء_بA2011ؤêب«اٍنNتغî~¸كك_¼s30ƒ|أہشھ£¬تاب«اٍ؟¹°©ثژخïنNتغ¹عـٹ£¬°²¾Sح،؛ح؛صظگح،·ضءذµع¶،¢بخ»،£
،،،،،°شعéLذ§¸ة”_ثطîIسٍ£¬›]سذ‡ّ®aثژ…¢إc¸‚ ژ£¬ء_تدµؤإةء_ذہتا½^Œ¦µؤ،®´َہذ،¯£»¼´ت¹تاصû‚€¸ة”_ثطîIسٍ£¬إةء_ذہز²ئً´aص¼“ءث°ë±ع½ة½،£،±ڈVضفتذµع°ثبثأٌلtش؛ش؛éLزüںëکث×ٍبصŒ¦±¾ˆَس›صك±يت¾£¬ڈVضف°üہ¨ت،لt،¢ؤد·½لtش؛،¢ضذة½بش؛µب´َلtش؛¶¼شعسأإةء_ذہ£¬¶ّازثüشçژ×ؤêزر±»¼{بëڈVضف±û¸خéTجطلt±£ˆَنNثژئ·ض®ءذ،£
،،،،س›صكك€ڈؤضذة½´َŒW¸½Œظؤ[ءِلtش؛µأضھ£¬ةوتآµؤءيحâثؤ·N؟¹ؤ[ءِثژخïز²¶¼شع±»ئص±éت¹سأ،£
،،،،·ضخِ£؛
،،،،‡ّƒب²»ء¼·´‘ھةظ»ٍزٍسأثژ„©ء؟ذ،
،،،،Œ¦سع‡ّƒبح⌦ةدتِثژخï²»ء¼·´‘ھ¾ùسذ²»ح¬£¬تا·ٌك@ذ©ثژخïشع‡ّƒب¸ü°²ب«£؟Œ¦´ث£¬Œ£¼ز±يت¾£؛·Q²»ةد½^Œ¦،°°²ب«،±£¬µ«لtةْµؤ°رêP؛ح±O؟طµؤحêةئ؟ةزش±ـأâثژخïت¹سأ³ِ¬F‡ہضط،°أ“ـ‰،±،£
،،،،×ٍبص£¬ڈVضفتذµع°ثبثأٌلtش؛ش؛éLزüںëکث½é½Bصf£¬ء_تدثژخïشع‡ّƒبةدتذا°زر½›كMذذءث±¾حءبئعإR´²ش‡ٍ£¬ش‡ٍك^³جضذ°l¬Fµؤ²¢°l°Y•ز»‘ھŒ‘بëصfأ÷•ّ،£،°ز»°مص³£بث×î¶à°lةْذ©فp°Y²»ء¼·´‘ھ£¬µ«بç¹ûسذ»ùµA¼²²،£¬دٌجاؤٍ²،،¢¼×؟؛،¢رھز؛²،µبشعةي£¬³ِ¬F‡ہضط²»ء¼·´‘ھ£¬ةُضءضآثہµؤïLëU•¸ك؛ـ¶à،£،±ثû±يت¾£¬سأثژا°شu¹ہ»¼صكتا·ٌكm؛د£¬Œ¦سعسأثژ°²ب«إc·ٌئًضّ·ا³£ضطزھµؤ×÷سأ،£
،،،،´ثح⣬خز‡ّسأثژ•¸ù“»¼صكَwضطس‹ثمŒچëHثژخï„©ء؟£¬دàŒ¦سع‡ّح⣬ضذ‡ّبثµؤ؟‚َwسأثژ„©ء؟ك€تائ«ذ،µؤ£¬Œ£¼زصJ飬ك@»ٍز²تا²»ء¼·´‘ھˆَ¸و³ِ¬Fف^ةظµؤشزٍض®ز»،£
،،،،“س›صكءث½â£¬إR´²لtةْ»ٍ×oت؟بç¹û°l¬Fف^é‡ہضطµؤثژخï²»ء¼·´‘ھ»¼صك£¬±طيڑةد½»ˆَ¸و£¬×î½Kكf½»ضء‡ّ¼زثژخï²»ء¼·´‘ھ±Oœyدµ½y£¬¶ّ¸ù“¶à¼زلtش؛تصµ½µؤ¶¨ئع·´ًپذإد¢µأضھ£¬‡ّƒب³ِ¬Fء_تدسأثژ‡ہضط²»ء¼·´‘ھµؤتآ¼µؤ´_²»ثمج«¶à،£
،،،،،°²»ؤـصfخز‚ƒµؤ±Oœyدµ½yز»¶¨±ب„eبث²î»ٍتاéT™‘ف^µح£¬ثùزشŒ§ضآ²»ء¼·´‘ھˆَ¸و”µز²²»بçبث¼ز،£،±زüںëکثصJé،£¶ّüS¼t±ّض÷بخ„t±يت¾£¬¸÷لtش؛×ش¼؛µؤ±Oœyء÷³جتا·ٌحêةئ،¢لt×oبث†T°رêPتا·ٌ‡ہ¸ٌ£¬ز²ض±½سس°ي‘ضّ²»ء¼·´‘ھˆَ¸وµؤ³ِ t،£
،،،،½üؤêپيأ½َwˆَµہµؤء_تدثژخï²»ء¼·´‘ھتآ¼
،،،،2005ؤê
،،،،“بص±¾أ½َwˆَµہ£¬سذ2أûةظؤêزٍ·سأ،°ك_·ئ،±شى³ة¾«ةٌ®گ³££¬²¢×î½Kثہحِ،£
،،،،2010ؤê
،،،،“ˆَµہ£¬ضذ‡ّةد؛£”µت®خ»ہدبثسأ°²¾Sح،ضخ¯ںüS°ك׃ذش£¬ز°l•؛•rذشت§أ÷،£
،،،،2012ؤê
،،،،“ˆَµہ£¬أہ‡ّز»‚€»¼صكش®ضْي—ؤ؟ةودسë[²m‡ہضط²»ء¼·´‘ھ£¬ةو¼°ثہحِ²،ہ15161بث£¬ثژخï8؟î،£
|
|
|
|
- ،¾ذآآ„،؟ „¢¼خءل؛ْ±ّخاصص
- ؤل؟ثث¹»ٍ·إءض•ّ؛ہ
- ،¾تض™C،؟ t¢µؤث‡ذg؛أû
- œطـ°ظR؟¨ ح¬أûح¬ذصؤمخزثû
- ،¾ظR؟¨،؟ ‚€ذش×£¸£ثحگغبث
- د²ذإضئشىہثآ شSش¸×£¸£
- ،¾َwس،؟ ûœ؟×زر¼سأث»تٌR
- ذ،ح½مأأ²¢ءذµعز»
- ،¾أہإ®،؟ ؤذبث»éا°µؤœت‚ن
- إ®بث¶¼سذµؤ؟ةگغأطأـ
- ،¾ˆDâڈ،؟ ؟ةگغاéبثإ®؛¢
- ء÷ذذâڈآ•دآفd تض™Cض÷î}
- ،¾²©؟ح،؟ شآذ½5ا§شعةد؛£
- ضط‘c‡ّëHذ،½ما°ب¼×شâظ|زة
- ،¾سخ‘ٍ،؟ iphoneسخ‘ٍدآفd
- ںلرھإcکsز« ²¶ô~ض®؛£µ×“ئ